8月30日,国家药监局药品审评中心关于发布《注册分类4、5.2类化学仿制药(口服固体制剂)生物等效性研究批次样品批量的一般要求(试行)》。
▍国家药监局,对一致性评价提要求
核心目的,是保证商业化生产批次样品,与生物等效性研究批次样品质量与疗效的一致性。
药品审评中心要求,对于片剂和胶囊剂(包括缓释制剂、咀嚼片、口崩片等),BE研究批次样品批量(以投料量计,下同)应不得低于10万制剂单位。
对于散剂、颗粒剂,BE研究批次样品批量应不得低于拟定商业化生产批量的1/10。
不符合上述要求的,应按照上述要求进行批量放大的补充研究。原则上,放大研究应在同一生产线上进行。如生产设备发生改变,生产设备的工作原理应保持一致。
▍防止一致性评价做成“一次性评价”
国家药监局表示,本技术要求自公布之日起正式实施,正式实施日期后启动BE研究的品种如样品批量不符合要求,将不予认可。
有行业人士表示,此次国家药监局药品审评中心的目的,不但要求一致性评价的“试验品”和原研药一致,流向市场的药品也应如此。防止一致性评价做成“一次性评价”。
此前在一次行业大会上,一位医保局的官员就对这种隐患表示了担忧,笔者在和业内人士的交流中,得到的反馈也是认为存在“一次性评价”的可能。
希望能把这个“口子”堵上。
▍又有8药品,通过一致性评价
根据原国家食药监总局在2016年公布的《2018年底前须完成仿制药一致性评价品种目录》要求,289种仿制药在2018年底前要完成一致性评价。如今,距离年底仅剩4个月的时间。
据米内网统计,自第五批一致性评价名单公布至今,又有8个仿制药通过一致性评价,享受政策红利。
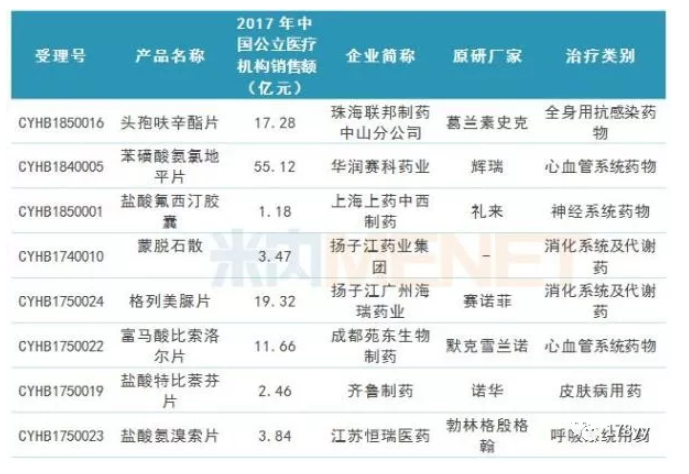
(来源:米内网数据库,数据统计截至8月31日)
▍“289品种”,通过16个
2017年7月开始,陆续有企业开始申报一致性评价,CDE每月承办的受理号平均为16个左右。但是从2018年5月开始,一致性评价申请受理号出现大幅度增长, CDE在审评审批方面的速度也加快了。
从“289品种”一致性评价进展看,331个受理号中,有139个受理号属于“289品种”,涉及品种数51个,其中通过一致性评价的受理号有29个,涉及品种16个,不批准通过一致性评价的受理号有2个,涉及品种2个。
以上就是仿制药一致性评价公司-桐晖药业小编分享的有关“又有8药品通过一致性评价”的全部内容,供大家参考!
广州市桐晖药业有限公司是一家符合现代化管理要求的GSP公司,在进口原料药细分领域是为业界翘楚,为客户提供专业的从药学研发、临床预BE到临床BE的药厂研发一站式解决方案。目前的重点业务主要包括:原料药联合申报、参比制剂一次性进口、临床预BE/正式BE和一致性评价服务。如需合作,欢迎来电咨询!
本文关键词:仿制药一致性评价,一致性评价公司